유전자 발현 조절 네트워크의 IPMK·SRF 역할 규명
[세종=뉴스핌] 이경태 기자 = 한국과학기술원(KAIST)은 생명과학과 김세윤 교수, 이광록 교수, 조원기 교수 공동연구팀이 동물 세포의 유전자 발현을 조절하는 핵심적인 원리를 규명했다고 22일 밝혔다.
연구팀은 다양한 암 발생 및 전이 현상, 줄기세포의 조직 분화, 신경 세포 활성화 과정을 근본적으로 유도하는 유전자 발현 조절 단백질의 핵심 유전자 발현 네트워크를 발견했다.
연구팀은 이노시톨 대사 효소에 의해 생성되는 이노시톨 인산 대사체가 진핵 세포의 신호전달 시스템에서 다양한 이차 신호전달물질로 작용하여, 암, 비만, 당뇨, 신경계 질환에 깊이 관여한다고 설명했다.
이들은 이노시톨 대사 시스템의 핵심 효소인 IPMK 단백질이 동물 세포의 주요 유전자 발현 네트워크의 전사 활성화 인자로 역할을 해낸다는 사실을 밝혔다.
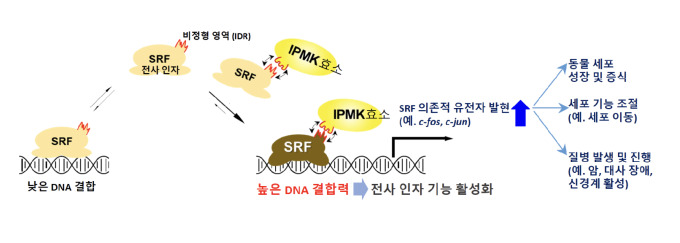
IPMK 단백질은 포도당과 유사한 대사 물질로서 유전자 발현을 직접 조절하는 기능을 갖고 있다. IPMK 효소는 전사 인자 SRF에 의한 유전자 전사 과정에서 중요한 역할을 한다. 그동안 작용 기전은 알려지지 않았으나, 이번 연구를 통해 이의 메커니즘이 밝혀졌다.
연구팀은 IPMK 단백질이 SRF 전사 인자와 직접 결합하여 SRF의 3차원 구조를 변화시킨다고 전했다. 이를 통해 IPMK 효소에 의해 활성화된 SRF 전사 인자가 다양한 유전자의 전사 과정을 촉진하는 데 기여함을 규명했다.
연구팀은 IPMK 효소와 SRF 전사 인자 간 결합 문제가 발생하면 SRF의 기능과 활성이 저하되어 유전자 발현에 심각한 장애가 생긴다는 사실을 최종적으로 확인했다.
이들은 특히 SRF 전사 인자의 비정형 영역이 중요한 조절 부위임을 밝혀, 비정형 단백질의 생물학적 중요성을 입증했다고 강조했다. 이러한 비정형 영역은 특별한 단백질 구조가 없이 존재하며, 이로 인해 학계의 주목을 받고 있다.
김세윤 교수는 이번 연구가 IPMK 단백질의 역할과 메커니즘을 증명한 중요한 성과라고 말하며, SRF 전사 인자로부터의 다양한 암 발생과 줄기세포의 조직 분화, 신경 세포 활성화 과정에 대한 이해가 혁신적인 치료 기술 개발에 기여할 것이라는 기대를 밝혔다.
이 연구 결과는 세계적 국제학술지 '핵산 연구'에 1월 7일 게재됐다.
이번 연구는 한국연구재단과 서경배과학재단, 삼성미래기술육성사업의 지원을 받아 수행됐다.
biggerthanseoul@newspim.com























